1. De hiv-epidemie in België
i. Trends in de hiv-diagnoses
Na de dalende trend van het aantal nieuwe hiv-diagnoses tussen 2012 en 2018, werd in 2019 een epidemiologisch plateau bereikt. Tussen 2019 en 2020 daalde het aantal nieuwe hiv-diagnoses met 21%. Deze sterke daling was duidelijk gerelateerd aan de COVID-19 pandemie en de maatregelen om de circulatie van het COVID-19 virus in te perken. Beide hadden een invloed op hiv-testactiviteiten, seksueel gedrag en migratiedynamieken.
In 2020 werden 727 nieuwe hiv-diagnoses vastgesteld, wat overeenstemt met 2 nieuwe diagnoses per dag. België blijft hiermee één van de West-Europese landen met in verhouding het hoogst aantal nieuwe hiv-diagnoses (6.3/100 000 inwoners)1.
Sinds het begin van de hiv-epidemie in België worden twee sleutelpopulaties bijzonder getroffen, met name mannen die seks hebben met mannen (MSM), met Belgische nationaliteit en heteroseksuele mannen en vrouwen afkomstig uit Sub-Saharaans Afrika. Gezien de dalende trend van de diagnoses in deze sleutelpopulaties wordt het aandeel van populaties met andere profielen de laatste jaren relatief groter en is de epidemie in België nu meer gediversifieerd. In 2020 werd 40% van de nieuwe hiv-diagnoses vastgesteld bij Belgische mannen die seks hebben met mannen en heteroseksuelen afkomstig van Sub-Saharaans Afrika.
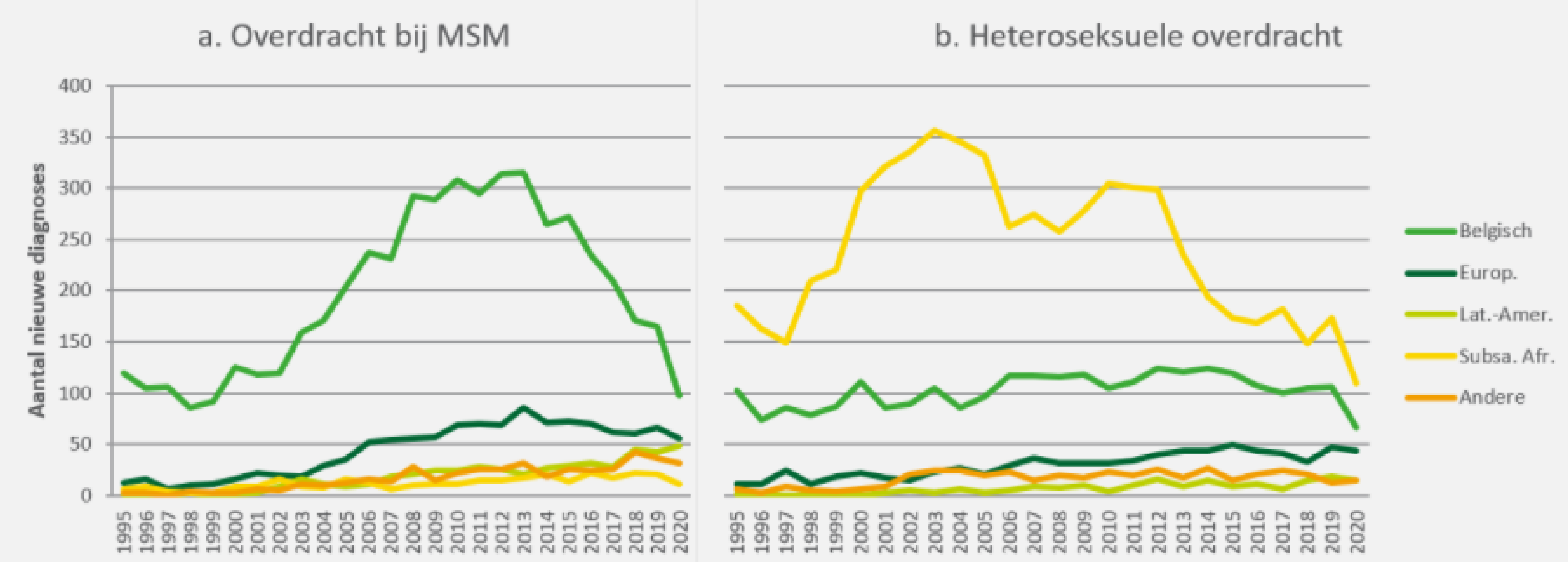
De neerwaartse trend van het aantal nieuwe hiv-diagnoses bij Belgische mannen die seks hebben met mannen werd in 2020 verdergezet; er was een lichte stijging bij mannen die seks hebben met mannen afkomstig uit Latijns-Amerika. Bij heteroseksuelen van Sub-Saharaanse Afrikaanse afkomst leek de dalende trend in 2019 gestopt te zijn, maar deze heeft zich in 2020 hernomen; er was eveneens een daling bij heteroseksuelen met de Belgische nationaliteit (figuur 1).
Figuur 1: Evolutie van het aantal nieuwe hiv-diagnoses per manier van overdracht en nationaliteit, België 1995-2020
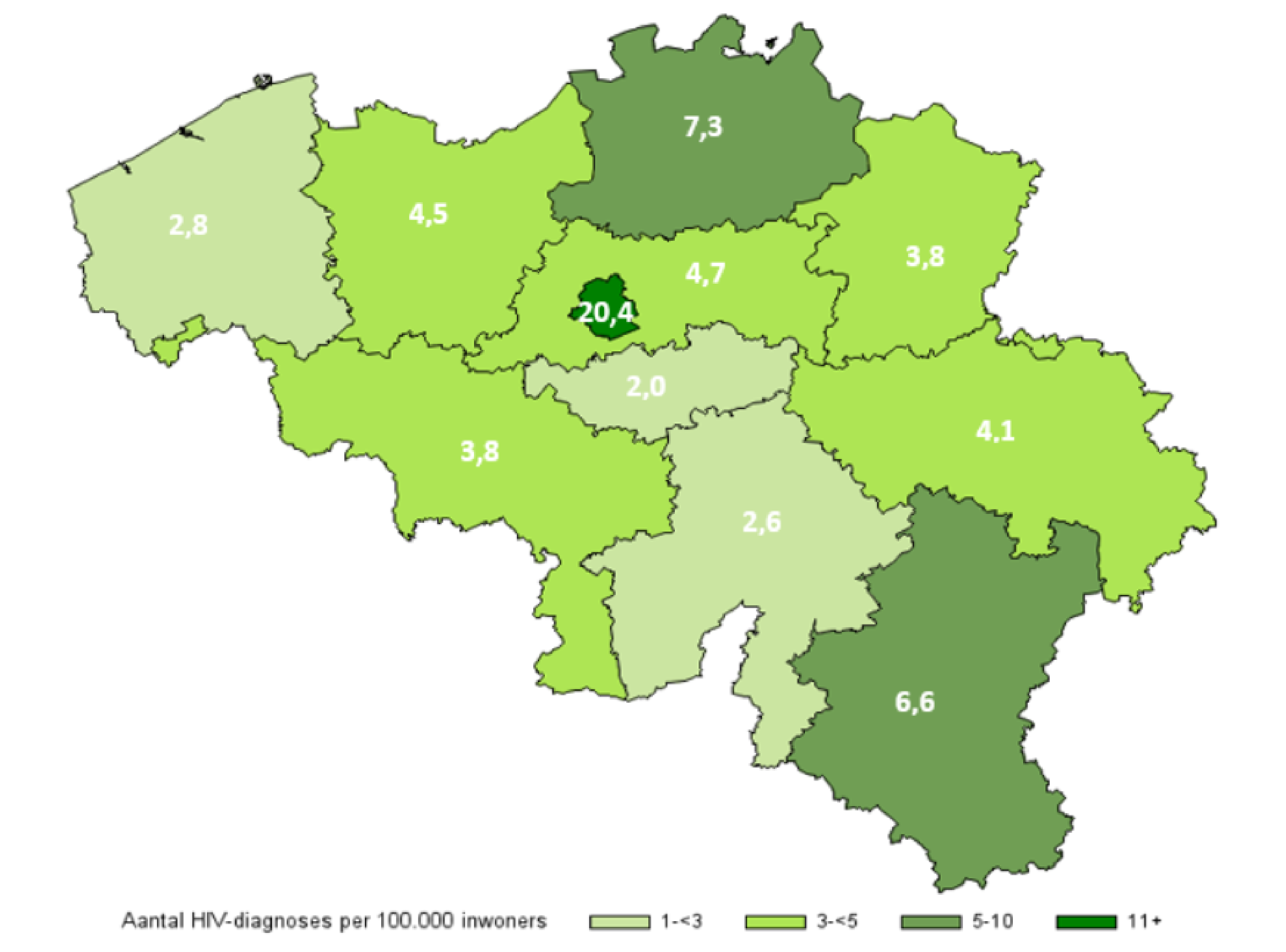
Wat betreft de geografische spreiding werd in 2020 het grootste aantal hiv-diagnoses gerapporteerd in het Brussels Hoofdstedelijk Gewest met 20.4 nieuwe diagnoses per 100 000 inwoners (figuur 2). Het aantal diagnoses was hoger in de steden (12.3 diagnoses per 100 000 inwoners) dan in de agglomeraties en de voorsteden (3.5 per 100 000 inwoners) of in dunbevolkte gebieden (2.6 per 100 000 inwoners). Het hoger aantal diagnoses in Brussel lijkt dus enerzijds verband te houden met het stedelijk karakter van het gewest en anderzijds met de specifieke kenmerken van de hoofdstad.
Figuur 2 : Aantal hiv-diagnoses per 100 000 inwoners en per provincie en Brussels Hoofdstedelijk Gewest, 2020
ii. Test- en diagnoseproces
De laattijdige hiv-diagnose vormt nog altijd een probleem, aangezien een hiv-infectie niet noodzakelijk tot een onmiddellijke diagnose leidt. Het tijdstip van de diagnose wordt beïnvloed door allerlei factoren, zoals het langzame verloop van de ziekte en ook de beschikbaarheid en de frequentie van testactiviteiten. In 2020 werd 36% van de hiv-infecties laattijdig vastgesteld (<350 CD4 /mm³ op het moment van de hiv-diagnose). Het aantal laattijdige diagnoses is in 2020 gedaald maar blijft vaker voorkomen bij heteroseksuelen (47%) dan bij mannen die seks hebben met mannen (22%).
In 2020 werd de helft van de hiv-tests in België uitgevoerd door huisartsen, die 42% van de hiv-diagnoses stelden.
iii. Geschat aantal mensen met hiv: met en zonder diagnose
In 2020 waren er in België naar schatting 18 753 mensen met hiv, wat neerkomt op een prevalentie van 1,7/1000 inwoners. Uit recent onderzoek bij de meest getroffen bevolkingsgroepen bleek de hiv-prevalentie bij migranten uit Afrika ten zuiden van de Sahara op 5,9% te liggen bij de vrouwen en op 4,2% bij de mannen2. Bij mannen die seks hebben met mannen ligt de gemelde hiv-prevalentie op 12%, zowel in het Sialon-onderzoek (op basis van biologische monsters)3 in Brussel als in het EMIS online-onderzoek (op basis van zelf gemelde gegevens) in België4.
Mensen met hiv (MMH) kunnen zich gedurende langere tijd voor hun diagnose niet bewust zijn van hun hiv-status. Mensen die seropositief zijn en niet beseffen dat ze hiv hebben, kunnen geen gebruik maken van een heel doeltreffende behandeling en kunnen ongewild bijdragen aan de verdere overdracht van de hiv-infectie. In 2020 waren naar schatting 1585 mensen zich niet bewust van hun hiv-infectie. Het geschatte aandeel van mensen met hiv dat zich niet bewust was van hun serostatus, daalde van 23,5% van de mensen met hiv in 2008 tot 8.5% in 2020. De hoogste prevalentie van niet-vastgestelde hiv-infecties was te vinden in de geografische regio’s met de grootste Belgische steden als bij mensen met een buitenlandse nationaliteit, voornamelijk mannen die seks hebben met mannen met een niet‐Europese nationaliteit5.
iv. De zorg voor mensen met hiv
Als gevolg van nieuwe infecties en de lage mortaliteit stijgt het aantal mensen met hiv met gemiddeld met 646 patiënten per jaar. In 2020 heeft zich uitzonderlijk een lichte daling voorgedaan van het aantal patiënten in medische follow-up ten gevolge van de COVID-19-pandemie. In 2020 werden in België 17 018 patiënten opgevolgd in de hiv-zorg. Een groeiend aandeel van de patiënten wordt ouder: van 19% van de patiënten van 50 jaar of ouder in 2006 tot 44% in 2020. Tegelijk zijn de patiënten intussen gemiddeld al langer geïnfecteerd en langer begonnen met ART en lopen ze daardoor een groter risico van (multi)comorbiditeit.
De indicatoren van de klinische zorg voor patiënten die worden opgevolgd in de hiv- referentiecentra (HRC’s) zijn heel goed: in 2008 nam 75% ART en dat percentage was in 2020 gestegen tot 98% van de patiënten en 98% van degenen die al minstens 6 maanden ART volgden hadden een onderdrukte virale lading (<200 kopieën/ml).
Een optimale zorg voor hiv-patiënten vereist continuïteit in de dienstverlening. Vanuit klinisch en volksgezondheidsoogpunt staan een vroegtijdige en volgehouden hiv-zorg en -behandeling voor virale onderdrukking, betere gezondheidsresultaten en minder risico’s van overdracht. De volgende factoren werden vastgesteld als risico voor een minder goede retentie in de hiv-zorg in België: een jongere leeftijd, intraveneus druggebruik, een recente diagnose en niet-Belg zijn. mannen die seks hebben met mannen hadden daarentegen een hogere retentiegraad6.
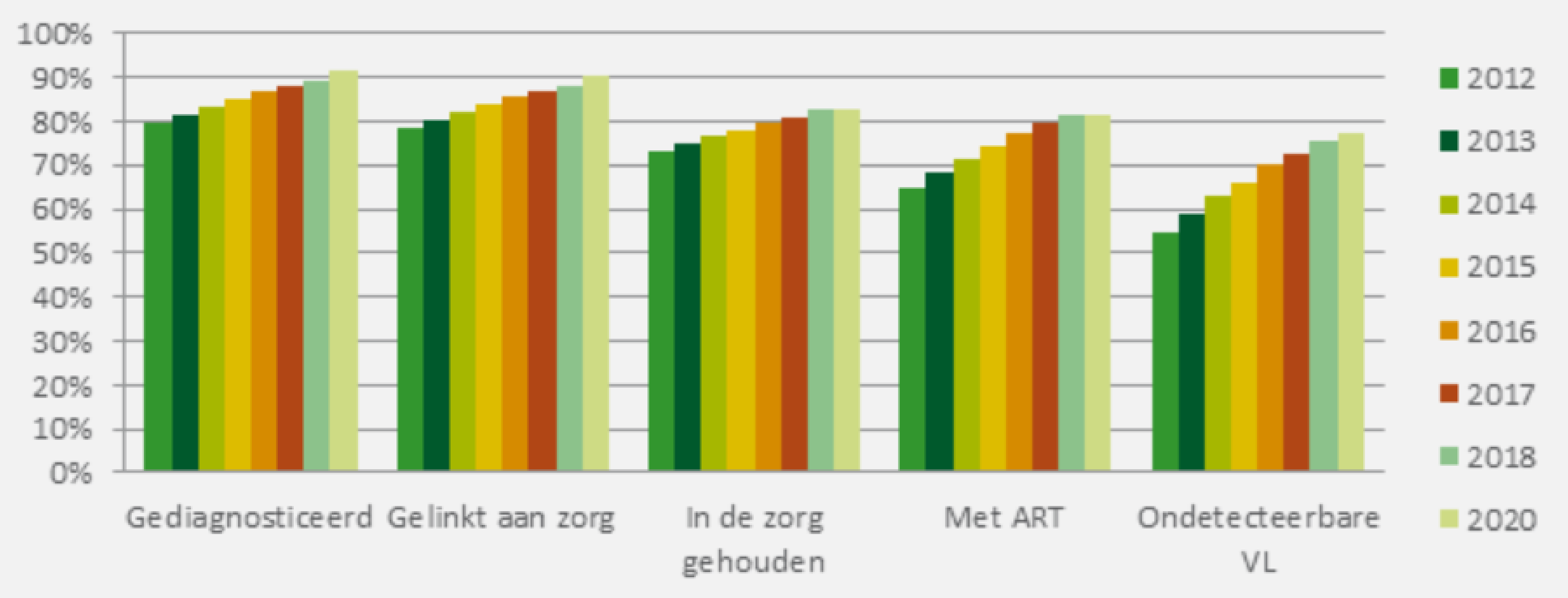
Het hiv-zorgcontinuüm is een monitoringkader dat gebruik maakt van transversale indicatoren voor het kwantificeren van het aantal mensen die een diagnose hebben gekregen, die zijn gekoppeld aan hiv-zorg, die een goede retentie in de zorg behouden, die ART krijgen en die een onderdrukte virale lading bereiken, in verhouding tot het geschatte aantal mensen met hiv. In 2020 had 92% van alle mensen met hiv in België een diagnose gekregen, was 90% gekoppeld aan hiv-zorg, bleef 83% in de zorg, kreeg 82% ART en had 77% een onderdrukte virale lading (figuur 3). In de loop der jaren is een verbetering in alle stadia van het continuüm vastgesteld, vooral voor het gebruik van ART en het onderdrukken van de virale lading.
Figuur 3: Hiv-zorgcontinuüm in België, 2012-2020
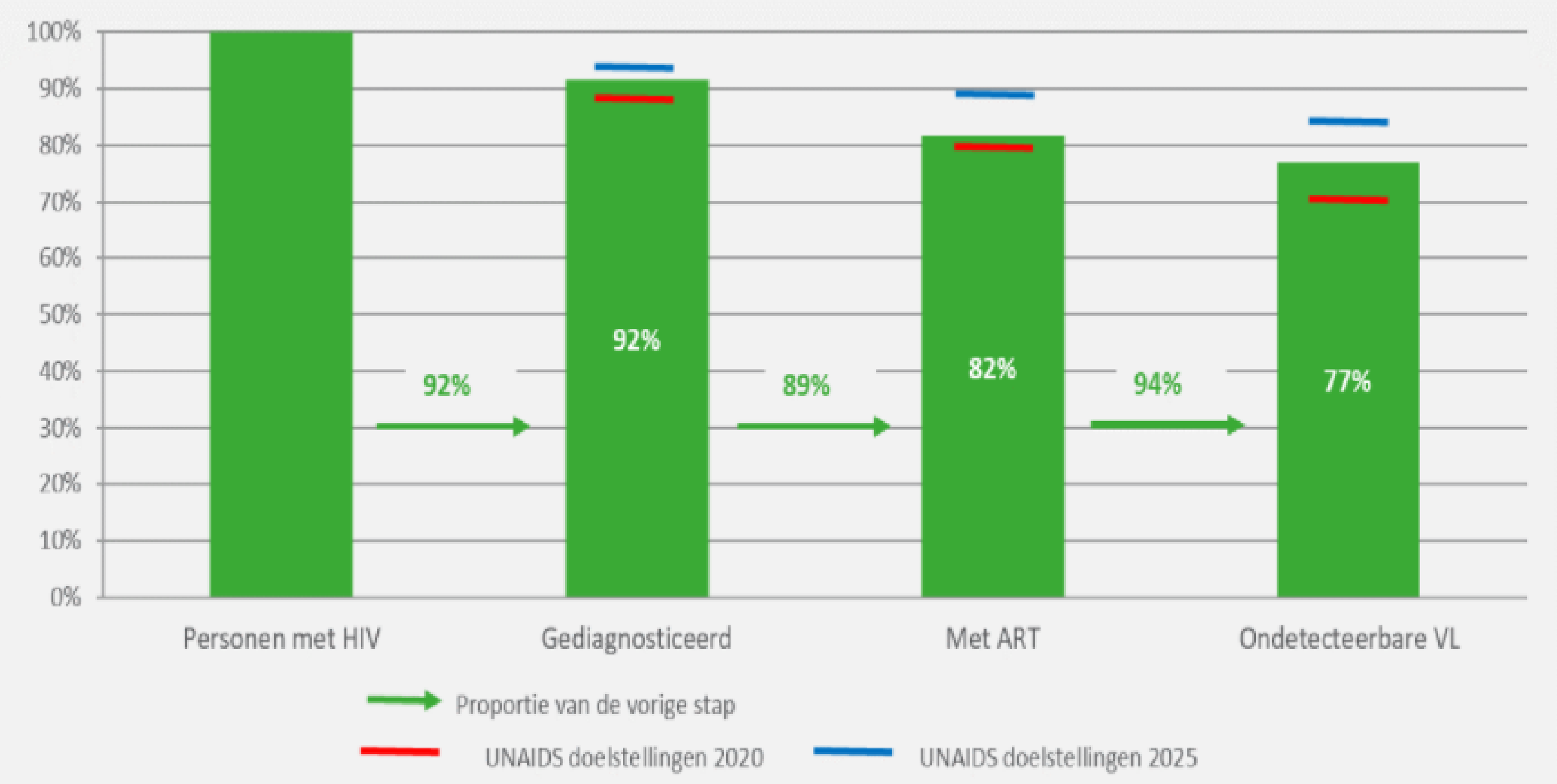
Voor 2020 heeft UNAIDS de ambitieuze 90-90-90 werelddoelstellingen opgesteld: 90% van de personen met hiv zou zijn of haar positieve serostatus moeten kennen, hiervan zou 90% antiretrovirale behandelingen moeten krijgen en hiervan zou 90% een ondetecteerbare virale lading moeten hebben. Zodra deze drieledige doelstelling is verwezenlijkt, zal de algemene doelstelling voor 2020 van minstens 73% van de personen die met hiv leven met een ondetecteerbare virale lading, bereikt zijn. België heeft deze algemene doelstelling gerealiseerd: in 2020 was 92% van de hiv-populatie gediagnosticeerd, hiervan kreeg 89% antiretrovirale behandelingen en hiervan had 94% een ondetecteerbare virale lading, of 77% van alle personen die met hiv leven (figuur 4). Bijkomende inspanningen om het aantal nieuwe infecties te beperken en te zorgen voor een vroegtijdige diagnose en voor de retentie in de zorg zullen bepalend zijn om in 2030 de volgende doelstellingen van 95-95-95 te bereiken.
Figuur 4 : Hiv-zorgcontinuüm in België in 2020 in vergelijking met de UNAIDS-doelstellingen
2. Verwante soa-epidemieën
i. Epidemiologische en gedragsdynamiek
Recent advies van deskundigen van het ECDC stelt dat het integreren van een strategie voor soa-preventie en -bestrijding binnen een hiv-strategie het meest logische en gunstige praktijkmodel is7. Verder wordt ook het integreren van een strategie voor virale hepatitis aanbevolen als bijkomende optie8.
De argumenten voor die integratie worden versterkt door de gemeenschappelijke overdrachtswijze , die leidt tot overlapping in de getroffen prioritaire doelgroepen. Op individueel vlak leidt dit tot co-infecties. Door de aanwezigheid van een soa zijn mensen kwetsbaarder voor hiv-infectie en een infectie met zowel hiv als een andere soa kan het risico van verdere hiv-overdracht vergroten. Op populatieniveau worden hiv- en soa-epidemieën aangedreven door een gelijkaardige epidemiologische dynamiek – het zijn zogenaamde syndemische epidemieën9. Door de inspanningen voor preventie en screening te bundelen, kan een synergistische aanpak worden gebruikt om hiv en soa’s effectiever en efficiënter te bestrijden.
Toch lopen niet alle doelgroepen die het meest getroffen worden door hiv hetzelfde risico op een soa. Net als in de meeste westerse landen is de vastgestelde algemene toename van syfilis- en gonorroe-diagnoses sinds 2002 in België vooral toe te schrijven aan de overdracht tussen mannen die seks hebben met mannen10 11.
Chlamydia, gonorroe en syfilis kennen een hoge prevalentie bij bepaalde subgroepen van mannen die seks hebben met mannen. Met betrekking tot het gedrag wordt deze hoge soa-prevalentie geassocieerd met een minder consequent condoomgebruik, het hebben van meerdere sekspartners en gebruik of afhankelijkheid van drugs. LGV (Chlamydia serovar L) en seksueel overgedragen hepatitis C worden in verhouding vaker vastgesteld bij seropositieve mannen die seks hebben met mannen. De infectie met hepatitis C houdt verband met specifieke risicovolle en traumatische seksuele praktijken zoals vuistneuken12.
Sinds de invoering van PrEP komen deze soa’s echter ook meer voor bij seronegatieve mannen die seks hebben met mannen die PrEP nemen13 14.
Soa’s zijn veel minder prevalent bij migranten uit Afrika ten zuiden van de Sahara dan bij mannen die seks hebben met mannen. Bij een recent onderzoek bij de gemeenschappen van Afrikanen afkomstig uit Sub-Saharaanse landen in de stad Antwerpen bleek dat soa-diagnoses geassocieerd zijn met een hiv-infectie.
ii. Gemelde gevallen15
Chlamydia is de vaakst voorkomende soa in België. Het aantal gemelde gevallen in België is gestegen van 9,5/100 000 inwoners in 2002 tot 77,0/100 000 inwoners in 2019. Maar die stijging ging ook gepaard met gevoeliger diagnosemethodes en meer gerichte en opportunistische tests bij risicogroepen. Op Europees niveau worden meer gevallen gemeld bij heteroseksuelen, vooral vrouwen. Toch wordt 10% van de gevallen van chlamydia vastgesteld bij mannen die seks hebben met mannen16. Tussen 2014 en 2019 is het aantal gevallen van LGV (Chlamydia serovar L) bij mannen die seks hebben met mannen gestaag toegenomen in België.
Gonorroe kende sinds 2002 een stijgende trend van 2,6/100 000 inwoners in 2002 tot 26.0/100 000 inwoners in 2019. In 2019 werd gonorroe vooral vastgesteld bij mannen tussen 20 en 39 jaar. Op Europees niveau en in landen met een gelijkaardige sociale en epidemiologische context zoals Nederland wordt tot 50% van de gevallen vastgesteld bij mannen die seks hebben met mannen17.
Ook Syfilis kende in België tijdens dezelfde periode (2002-2019) een toename, van 0,4/100 000 inwoners in 2002 tot 21,6/100 000 inwoners in 2019. In 2019 werd syfilis vooral vastgesteld bij mannen tussen 20 en 59 jaar. Uit Europese gegevens over de overdracht van syfilis blijkt dat tot 75% van de gevallen wordt vastgesteld bij mannen die seks hebben met mannen18.
3. Prioritaire doelgroepen
Mannen die seks hebben met mannen en Sub-Saharaans Afrikaanse migranten zijn de bevolkingsgroepen die het meest getroffen worden door de Belgische hiv-epidemie. Maar niet alle mensen uit die zwaarst getroffen groepen lopen hetzelfde risico: de dynamiek van de hiv-overdracht hangt af van de invloed van de verschillende risico- en kwetsbaarheidsfactoren waaraan zij zijn blootgesteld en die elkaar onderling versterken.
Om die reden spitst het hiv-plan zich toe op prioritaire doelgroepen, die worden omschreven als groepen die door een specifiek hoger risicogedrag en contextuele kwetsbaarheden een hoger risico op hiv en verwante soa’s lopen. Die doelgroepen zijn heel belangrijk voor de hiv-epidemie en ook voor de hiv-aanpak in België. Het gaat om mannen die seks hebben met mannen, migranten (zonder papieren) uit landen met een hoge hiv-prevalentie, transgenders, sekswerkers, mensen die intraveneus drugs gebruiken en gedetineerden. Binnen elke prioritaire doelgroep hebben jongeren specifieke leeftijds- of ontwikkelingsgebonden behoeften en de acties van het hiv-plan zullen daar rekening mee houden.
Om de prioritaire doelgroepen voor hiv te bereiken, moet daarom worden ingegrepen op een combinatie van kwetsbaarheidsfactoren, zoals onvoldoende toegang tot gezondheidszorg, multifactoriële en intersectionale discriminatie, stigmatisering omwille van hiv en sociaaleconomische ongelijkheid.
Hoewel er hulpmechanismen bestaan om universele gezondheidszorg te waarborgen, bijvoorbeeld via de procedure van dringende medische zorg, kunnen complexe administratieve procedures toch een belangrijke belemmering vormen voor de reële toegankelijkheid van diensten. België biedt ook een sterk en progressief regelgevend kader op het vlak van discriminatie, dat – onder andere – beschermt tegen discriminatie op basis van gender, etniciteit, seksuele geaardheid of de huidige en toekomstige gezondheidstoestand19. Maar toch wordt de kwetsbaarheid voor hiv-infectie nog altijd vergroot door ervaren en daadwerkelijke stigmatisering en discriminatie omwille van hiv, als gevolg van culturele gewoonten, godsdienstige overtuigingen, wettelijke beperkingen en de criminalisering van de hiv-overdracht. Naast of vervlochten met stigmatisering en discriminatie omwille van hiv kunnen mensen met hiv te maken krijgen met stigmatisering en discriminatie omwille van ras, seksuele geaardheid of genderidentiteit. Door discriminatie en (zelf)stigmatisering kan het gebeuren dat mensen met hiv geen toegang zoeken tot zorg en zichzelf uitsluiten van sociale hulp20.
Bovendien worden bepaalde prioritaire doelgroepen geconfronteerd met armoede en hebben zij maar beperkte toegang tot essentiële diensten als huisvesting, onderwijs, werkgelegenheid, bescherming en justitie21. Die factoren brengen een bijkomende kwetsbaarheid met zich mee, omdat ze de controle over de seksuele gezondheid ondermijnen en het risico van seksueel geweld en praktijken van transactionele seks vergroten. Ook het verband tussen migratie, armoede en hiv wordt wereldwijd erkend. Onderzoek in België heeft uitgewezen dat hiv-infectie bij Sub-Saharaans Afrikaanse migranten verband houdt met sociaaleconomische kwetsbaarheid, naast gelijktijdige relaties en seksuele betrekkingen vooral binnen Afrikaanse seksuele netwerken22. Er is ook vastgesteld dat sub-Saharaans Afrikaanse migranten mobiel zijn en tijdens die mobiliteit seksueel risicogedrag kunnen vertonen , waardoor het risico van hiv-infectie na de migratie toeneemt23.
Een aantal goede praktijken heeft uitgewezen dat interventies die zich rechtstreeks richten tot prioritaire doelgroepen positieve resultaten kunnen opleveren. In de Belgische context is het dankzij harm reduction-diensten mogelijk geweest om de impact van hiv bij mensen die intraveneus drugs gebruiken vrij laag te houden in vergelijking met andere landen. De doeltreffende preventieve aanpak ten aanzien van – maar ook door – sekswerkers heeft niet enkel het risico van hiv- en soa-infecties verminderd, maar beoogde ook andere verwante risico’s, zoals geweld, te verminderen. Daarnaast hebben verschillende doelgroeporganisaties deskundigheid ontwikkeld in het werken via een participatieve aanpak, in nauwe samenwerking met de getroffen commmunities,. Dit zorgde ervoor dat de vraag naar preventie door de betreffende doelgroepen en het gevoel van betrokkenheid tot zelfs eigenaarschap van bijkomende diensten, zoals lotgenotensteun, toenam.
Samengevat kunnen we stellen dat er voortdurende interventies nodig zijn om de toegang tot diensten voor hiv-preventie en -zorg te verbeteren. Brede programma’s voor hiv-preventie moeten zich niet alleen toespitsen op de biologische oorzaken van hiv-infectie, maar ook op de sociale context en de structurele factoren die het seksueel handelen en het gezondheidsbevorderend gedrag beïnvloeden. Doeltreffend strijden tegen hiv betekent de mensenrechten verdedigen en alle vormen van discriminatie bestrijden en ook werken vanuit een multisectorale benadering om de sociaaleconomische ongelijkheid aan te pakken.
4. Overzicht van de hiv-actoren
i. Organisaties voor hiv-preventie en -hulp
Diverse organisaties die werken aan gezondheidspromotie, preventie en ondersteuning voeren activiteiten uit voor de prioritaire doelgroepen die getroffen worden door hiv. Het gaat om organisaties die een of meer van de onderstaande diensten bieden:
- Algemene hulpverlening voor prioritaire doelgroepen zoals sekswerkers, LGBTQI, migranten, mensen die intraveneus drugs gebruiken en gedetineerden;
- Informatieverstrekking over hiv en soa’s en preventieve diensten voor het brede publiek of groepen met een verhoogd risico op een hiv-infectie;
- Structurele pleitbezorging voor het verdedigen en beschermen van de rechten van mensen die (sociaal/structureel) risico lopen van stigmatisering en discriminatie;
- Rechtstreekse hulpverlening aan mensen die zijn getroffen door/leven met hiv, via peer-to-peer support, informatie en begeleiding.
ii. Hiv-referentiecentra
De Belgische hiv-referentiecentra (HRC’s) zijn door de overheid erkende expertisecentra. Een HRC is verbonden aan een ziekenhuis en biedt toegankelijke en multidisciplinaire zorg voor mensen met hiv, zoals medische behandeling en zorg, psychosociale hulp en soa-screening. De erkende HRC’s hebben een conventie met het Rijksinstituut voor Ziekte- en Invaliditeitsverzekering (RIZIV), waardoor de medische behandeling en ook de multidisciplinaire zorg en hulp terugbetaalbaar zijn. Sinds 2017 zijn de HRC’s ook verantwoordelijk voor het verlenen van PrEP-diensten. Er zijn twaalf erkende HRC’s in België, verspreid over het hele grondgebied om de toegankelijkheid van deze gespecialiseerde zorg te verzekeren. Vijf van de erkende HRC’s bevinden zich in Vlaanderen (Antwerpen, Leuven, Hasselt, Gent, en Brugge), vier in Brussel (UZ Brussel, Sint-Pieters, Erasmus en Sint-Lukas) en drie in Wallonië (Luik, Charleroi en Namen).
iii. Aids-referentielaboratoria
De Belgische aids-referentielaboratoria (ARL’s) zijn expertisecentra opgericht in 1987. Ze werken nauw samen met de hiv-referentiecentra. Er zijn drie ARL’s in Vlaanderen (Antwerpen, Gent en Leuven), drie in Brussel (Jette, Sint-Lukas en Erasmus) en een in Wallonië (Luik). Hun taak bestaat erin hiv-infecties te bevestigen of uit te sluiten in geval van een reactieve screeningtest. Ze voeren ook de analyses uit voor de laboratoriummonitoring van hiv-infecties zoals het testen van de virale lading en onderzoek van medicatieresistentie. ARLs beoordelen eveneens de kwaliteit van tests die worden gebruikt voor diagnose en voor de opvolging van hiv-patiënten. Tenslotte documenteren ze nieuwe infecties zodat epidemiologische analyses en wetenschappelijk onderzoek mogelijk zijn. Voor dat laatste werken de laboratoria nauw samen met Sciensano. De ARL’s worden gefinancierd via een conventie met het RIZIV.
iv. Laagdrempelige screeningcentra
Op basis van het Koninklijk Besluit van 6 maart 2017 (voorheen het Koninklijk Besluit van 28 december 2006) financiert het RIZIV drie HRC’s als laagdrempelige screeningcentra: het Elisa Centrum in het HRC Sint-Pieter; Sida Sol vzw in het HRC Luik en het Helpcenter in het HRC Antwerpen. De screening waarnaar in de context van dit Koninklijk Besluit wordt verwezen, is bedoeld voor iedereen die een verhoogd risico loopt van infectie met hiv of een soa en die behoort tot een of meer van de volgende doelgroepen:
- migranten uit een land met een hiv-prevalentie die minstens 10 keer hoger ligt dan de hiv-prevalentie in België;
- mannen die seks hebben met mannen;
- intraveneuze druggebruikers en hun partners;
- sekswerkers en hun partners;
- klanten van sekswerkers en hun partners;
- mensen die onbeschermde seksuele betrekkingen hebben buiten de context van een permanente relatie;
- mensen die meerdere partners hebben of die seks hebben met een partner die meerdere partners heeft.
Die personen kunnen een gratis (en anonieme) hiv-test krijgen, indien nodig aangevuld met een soa-screening. De screeningactiviteiten kunnen buiten het screeningcentrum gebeuren (gedecentraliseerd testen), om ze beter toegankelijk te maken voor de doelgroepen.
v. Sciensano
Sciensano, het Belgisch Instituut voor Gezondheid, is bevoegd voor de epidemiologische surveillance van hiv en aids in België. Daartoe verzamelt Sciensano meldingen van nieuwe hiv-diagnoses van de ARL’s en van nieuwe aidsgevallen door clinici. Sinds 2006 verzamelt Sciensano ook individuele routinegegevens over hiv-patiënten die medisch worden opgevolgd door de HRC’s en de ARL’s: dit is de Belgische hiv-cohorte. In 2018 werd ook de monitoring van PrEP- en PEP-gebruikers opgenomen in de hiv-surveillance.
Soa’s als chlamydia, gonorroe en syfilis en ook enkele andere soa’s worden door Sciensano gemonitord via verschillende surveillancebronnen.
vi. BREACH
BREACH, het Belgisch Onderzoeksconsortium voor aids en hiv, is een gezamenlijk initiatief van de Belgische hiv-referentiecentra, aids-referentielaboratoria, wetenschappelijke onderzoeksgroepen en belangenorganisaties op het terrein van hiv-infectie en aids. BREACH wil het Belgisch hiv-onderzoek van alle aard (klinische trials, epidemiologie, volksgezondheid, fundamenteel en translationeel onderzoek, gezondheidseconomie) bevorderen en ondersteunen, zowel op nationaal als op internationaal vlak en de algemene zichtbaarheid ervan verhogen. In dat kader worden jaarlijkse symposia en wetenschappelijke bijeenkomsten georganiseerd. BREACH telt ook een Werkgroep Volksgezondheid en een PrEP Task Force; de beide platforms bieden gelegenheid tot uitwisseling en samenwerking.
--------------------------------------------------
1 Sasse A, Deblonde J, De Rouck M, Montourcy M, Van Beckhoven D. Epidemiology of AIDS and HIV infection in Belgium. Sciensano; 2020. Nederlandstalige versie beschikbaar via: https://doi.org/10.25608/5c9n-4t26
2 Loos J, Nöstlinger C, Vuylsteke B, Deblonde J, Ndungu M, Kint I, Manirankunda L, Reyniers T, Adobea D, Laga M, Colebunders R. First HIV prevalence estimates of a representative sample of adult sub-Saharan African migrants in a European city. Results of a community-based, cross-sectional study in Antwerp, Belgium. PloS one. 2017;12(4). Te raadplegen via: https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0174677
3 The Sialon II Project. Report on a Bio-behavioural Survey among MSM in 13 European cities. ISBN 978-88-98768-55-4 Cierre Grafica, 2016. Editors: Massimo Mirandola, Lorenzo Gios, Nigel Sherriff, Igor Toskin, Ulrich Marcus, Susanne Schink, Barbara Suligoi, Cinta Folch, Magdalena Rosińska. Te raadplegen via: http://www.sialon.eu/data2/file/133_Sialon%20II_Report%20on%20a%20Bio-behavioural%20Survey%20among%20MSM%20in%2013%20European%20cities.pdf
4 Schmidt AJ, Weatherburn P, Hickson F. The EMIS-Network. EMIS 2017 – The European Men-Who-Have Sex-With-Men Internet Survey. Key findings from 50 countries. Stockholm: ECDC 2019
5 Marty L., Van Beckhoven D., Ost C., Deblonde J., Costagliola D., Sasse A., Supervie V. and the HERMETIC Study Group. Estimates of the HIV undiagnosed population in Belgium reveals higher prevalence for MSM with foreign nationality and for geographic areas hosting big cities. JIAS. 2019, 22:e25371. Available at : https://doi.org/10.1002/jia2.25371
6 Van Beckhoven D, Florence E, De Wit S, Wyndham-Thomas C, Sasse A, Van Oyen H, Macq J; Belgian Research on AIDS, HIV Consortium (BREACH). Incidence rate, predictors and outcomes of interruption of HIV care: nationwide results from the Belgian HIV cohort. HIV Med. 2020 Oct;21(9):557-566. doi: 10.1111/hiv.12901. Epub 2020 Jul 5. PMID: 32627351; PMCID: PMC7540395.
7 European Centre for Disease Prevention and Control. Developing a national strategy for the prevention and control of sexually transmitted infections. Stockholm: ECDC; 2019. Available through: https://www.ecdc.europa.eu/sites/default/files/documents/strategies-to-control-STIs.pdf
8 European Centre for Disease Prevention and Control. Public health guidance on HIV, Hepatitis B and C testing in the EU/EEA - an integrated approach. Stockholm: ECDC; 2018. Available through: https://www.ecdc.europa.eu/sites/default/files/documents/hiv-hep-guidance-brief-6-december.pdf
9 Singer M, Bulled N, Ostrach B, Mendenhall E. Syndemics and the biosocial conception of health. The Lancet. 2017 Mar 4;389(10072):941-50
10 European Centre for Disease Prevention and Control. Gonorrhoea. In: ECDC. Annual epidemiological report for 2017. Stockholm: ECDC; 2019.Available through: https://www.ecdc.europa.eu/sites/default/files/documents/gonorrhoea-annual-epidemiological-report-2017.pdf
11 European Centre for Disease Prevention and Control. Syphilis. In: ECDC. Annual epidemiological report for 2017. Stockholm: ECDC; 2019. Available through: https://www.ecdc.europa.eu/sites/default/files/documents/syphilis-annual-epidemiological-report-2017.pdf
12 Apers L, Vandenberghe W, De Wit S, Kabeya K, Callens S, Buyze J, et al. Risk factors for HCV acquisition among HIV-positive MSM in Belgium. JAIDS J Acquir Immune Defic Syndr. 2015;68(5):585–593.
13 Sasse A, Deblonde J, De Rouck M, Montourcy M, Van Beckhoven D. Epidemiology of AIDS and HIV infection in Belgium. Sciensano; 2019. Dutch version available through: https://doi.org/10.25608/5c9n-4t26; French version available through: https://doi.org/10.25608/k6sn-n789;
14 Vuylsteke, B., Reyniers, T., De Baetselier, I., Nöstlinger, C., Crucitti, T., Buyze, J., Kenyon, C., Wouters, K. and Laga, M., 2019. Daily and event-driven pre-exposure prophylaxis for men who have sex with men in Belgium: results of a prospective cohort measuring adherence, sexual behaviour and STI incidence. Journal of the International AIDS Society, 22(10), p.e25407
15 Vanden Berghe, W., De Baetselier, I., Van Cauteren, D., Sasse, A., Quoilin, S. Surveillances des infections sexuellement transmissibles. Données pour la période 2017-2019. Bruxelles, Belgique : Sciensano. Numéro de rapport : D/2020/14.440/85. Available through: https://www.sciensano.be/sites/default/files/report_sti_sciensano_1719_fr.pdf
16 European Centre for Disease Prevention and Control. Chlamydia infection. In: ECDC. Annual epidemiological report for 2017. Stockholm: ECDC; 2019. Available through: https://www.ecdc.europa.eu/sites/default/files/documents/AER_for_2017-chlamydia-infection.pdf
17 European Centre for Disease Prevention and Control. Gonorrhoea. In: ECDC. Annual epidemiological report for 2017. Stockholm: ECDC; 2019. Available through: https://www.ecdc.europa.eu/sites/default/files/documents/gonorrhoea-annual-epidemiological-report-2017.pdf
18 European Centre for Disease Prevention and Control. Syphilis. In: ECDC. Annual epidemiological report for 2017. Stockholm: ECDC; 2019. Available through: https://www.ecdc.europa.eu/sites/default/files/documents/syphilis-annual-epidemiological-report-2017.pdf
19 UNIA. The 19 grounds of discrimination. Available at: https://www.unia.be/en/grounds-of-discrimination/the-19-grounds-of-discrimination
20 Pezeril C. Lutte contre le SIDA et promotion de la santé sexuelle. Santé Conjuguée, 2019 n° 86. Available at: https://observatoire-sidasexualites.be/wp-content/uploads/SC-86-in-lgbt-def-pezeril.pdf
21 Gennotte et al. (2017). Oral presentation at the BEACH symposium 2017, Anderlecht; Belgium. Available at : http://www.breach-hiv.be/media/docs/BREACHSympo2017/AMASE,AFGennotteBreach3pourlesite.pdf
22 Loos J, Nöstlinger C, Vuylsteke B, Deblonde J, Ndungu M, Kint I, Manirankunda L, Reyniers T, Adobea D, Laga M, Colebunders R. First HIV prevalence estimates of a representative sample of adult sub-Saharan African migrants in a European city. Results of a community-based, cross-sectional study in Antwerp, Belgium. PloS one. 2017;12(4). Available at: https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0174677
23 Dias S, Gama A, Loos J, Roxo L, Simões D, Nöstlinger C (2020) The role of mobility in sexual risk behaviour and HIV acquisition among sub-Saharan African migrants residing in two European cities. PLoS ONE 15(2):e0228584. https://doi.org/10.1371/journal.pone.0228584
